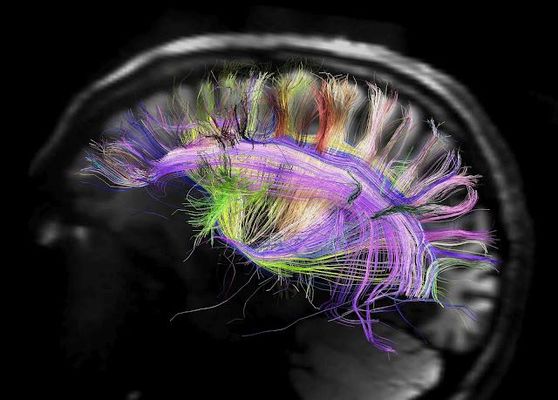
Al igual que los cables de fibra óptica que conectan teléfonos fijos, las ramas largas de las células del cerebro transmiten información de una neurona a la siguiente.
A diferencia de los cables telefónicos que solo pueden transmitir pasivamente señales eléctricas, sin embargo, las ramas neuronales están salpicadas de sinapsis, potencias computacionales activas que se reestructuran constantemente para formar nuestros pensamientos y recuerdos.
Para un neurocientífico deseoso de estudiar los circuitos neuronales y la función cerebral, las dendritas, los cables de entrada, son un lugar prometedor para comenzar. Pero con una anchura media decenas o cientos de veces menor que un cabello humano, las dendritas son difíciles de observar. A nivel nanoescala, las sinapsis están aún más lejos del alcance. Claro, los microscopios pueden ayudar a ampliar ópticamente el tejido, pero incluso el equipo más avanzado tiene una resolución limitada, y el estilo «zoom y mejorar» del estilo CSI o Mentes Criminales casi nunca funciona.
¿Y si, en lugar de explotar ópticamente el cerebro, pudiéramos hacerlo físicamente más grande?
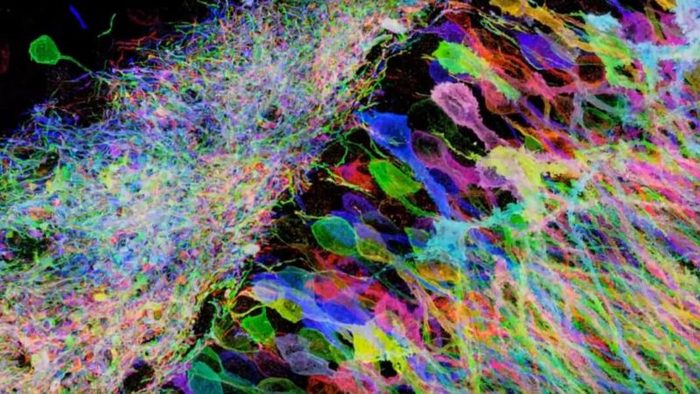
¿Suena como algo imposible? Nosotros también pensamos lo mismo. Pero esta semana, un equipo de neuroingenieros liderado por el Dr. Edward Boyden en el MIT ha logrado tal hazaña. Al incrustar el cerebro en un gel que se hincha cuando se bombea con agua, el equipo expandió el tejido cerebral del ratón a aproximadamente 20 veces su tamaño original, preservando la estructura normal y las conexiones de las neuronas y sus dendritas sin dañarlas.
Usando este método, acertadamente llamado microscopía de expansión (ExM), el equipo reconstruyó un pedazo minúsculo del cerebro del ratón en 3D. Normalmente, las dendritas se entrelazan en un lío desordenado, lo que hace difícil separar las conexiones sinápticas individuales con un microscopio óptico convencional.
Con ExM, los científicos se asomaron fácilmente a los rincones y recovecos de las dendritas, permitiendo una mirada sin precedentes a pequeñas protuberancias en forma de hongo llamadas espinas dendríticas, donde las sinapsis se sientan.
Incluso más heavy, el método también expuso grupos de proteínas individuales dentro de las espinas para apoyar la función de sinapsis normal y ayudar a crear circuitos neuronales.
«ExM se puede utilizar para explorar la conectividad neural en 3D con precisión espacial suficiente para resolver las conexiones sinápticas individuales«, seguran los autores.
«Si pudieras reconstruir un circuito completo del cerebro, tal vez podrías hacer un modelo computacional de cómo genera los fenómenos complejos como decisiones y emociones», dice Boyden, «podrías modelar la dinámica del cerebro«. (¡Qué miedo!)

Cartógrafos cerebrales
El mapeo cerebral ha sido el centro de la «gran neurociencia» durante los últimos años. Ambiciosos mil millones de dólares moonshots como la Iniciativa BRAIN y el Blue Brain Project de Europa se esfuerzan por desarrollar nuevos métodos que permitan a los neurocientíficos reconstruir en detalle el ratón y, en última instancia, el cerebro humano.
Estos proyectos provienen de un principio guía en biología: la forma engendra la función. Para entender y recrear un sistema eléctrico, el primer paso es retirar su plan de cableado. Del mismo modo, los científicos creen que el mapeo de las conexiones físicas y funcionales entre las neuronas es nuestra mejor opción para romper el funcionamiento básico del cerebro, su «código neural«.
Ciertamente ha habido algunas victorias de perfil alto en el dominio del mapeo cerebral. El mes pasado, un equipo internacional dio a conocer un procedimiento automatizado que descubrió una neurona sorprendentemente grande que rodea todo el cerebro del ratón.
Pero todos los esfuerzos de creación de gráficos cerebrales están limitados por la resolución del microscopio. Aunque los físicos han trabajado durante mucho tiempo cuáles son los parámetros más importantes para superar estos límites, mejorar la potencia y la calidad de los microscopios ha sido una batalla cuesta arriba.
Alicia en el país de las Maravillas
El equipo de Boyden adopta el enfoque opuesto: en lugar de luchar con la dispersión de la luz y la física, ¿por qué no agrandar la muestra biológica?
En el año 2015, su equipo demostró que dilatar el tejido cerebral (sin estallarlo en pedazos) es posible. La clave es utilizar cerebros que se han conservado en formalina, cortándola en secciones muy delgadas e inyectando cada sección con un gel denso, generado uniformemente gel hiperabsorbente utilizado normalmente en pañales para bebés.
Antes de la expansión, el equipo etiquetó las proteínas que querían que la imagen-por ejemplo, las proteínas en la sinapsis-con una molécula personalizada llamada un anticuerpo. En un extremo, el anticuerpo contiene un grupo químico que se une a los polímeros que forman el gel expandible, que ancla las proteínas marcadas al gel. En el otro extremo hay una pequeña hebra de ADN que actúa como un código de barras.
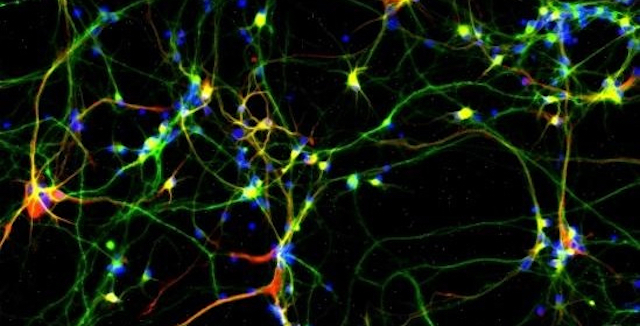
Después de etiquetarlo, el tejido se trata con un ablandador suave de carne para deshacer las proteínas que lo mantienen normalmente juntos. El equipo entonces colocó el gel cerebral en el agua y lo observó expandirse aproximadamente a cuatro veces y media su tamaño normal, permitiendo que las etiquetas se alejen unas de otras como puntos en un globo inflable.
Esta rebanada de cerebro ampliada está entonces lista para la obtención de imágenes con un tipo común de microscopio llamado microscopio confocal. Para visualizar las proteínas etiquetadas, los investigadores añadieron diferentes colores sondas fluorescentes que se unen a los códigos de barras de ADN; de esta manera, un tipo de proteína se etiqueta amarilla; otro verde; otro azul, y así sucesivamente.
El método permitió a los científicos lograr una resolución de aproximadamente 60 nanómetros, aproximadamente diez veces mayor que sin tratar el tejido.
Sin embargo, Boyden estaba insatisfecho.
«Las biomoléculas individuales son mucho más pequeñas que eso, digamos cinco nanómetros o incluso más pequeñas», dice. Y la expansión del tejido lo hizo aún más inestable y destruyó la estructura normal del cerebro.
A través del espejo
Para superar el límite de crecimiento, el equipo modificó su enfoque para que, después de la primera expansión, el cerebro-gel nuevamente se incrustara en un nuevo gel que hincha el tejido una segunda vez, algo que llaman «expansión iterativa«.
Centrándose en el hipocampo del ratón, una región del cerebro importante para el aprendizaje y la memoria, los investigadores podían distinguir claramente los contornos afilados de las dendritas y sus espinas. Sin embargo, cuando se trataba de las proteínas que componen las sinapsis, se presentaron como manchas borrosas poco.
En contraste, las proteínas sinápticas se etiquetaron en el tejido tratado con el nuevo iExM. No solo los investigadores podían ver las proteínas de «firma» que se encuentran en cada lado de la sinapsis, también podrían visualizar directamente los receptores neuroquímicos que se encuentran en las sinapsis. Estos receptores permiten que la información salte de una neurona a la siguiente actuando como parte de la maquinaria que transforma las señales eléctricas en las químicas.
De esta manera, los investigadores pueden ser capaces de mapear las configuraciones de receptor únicas que conectan y desconectan circuitos neuronales.
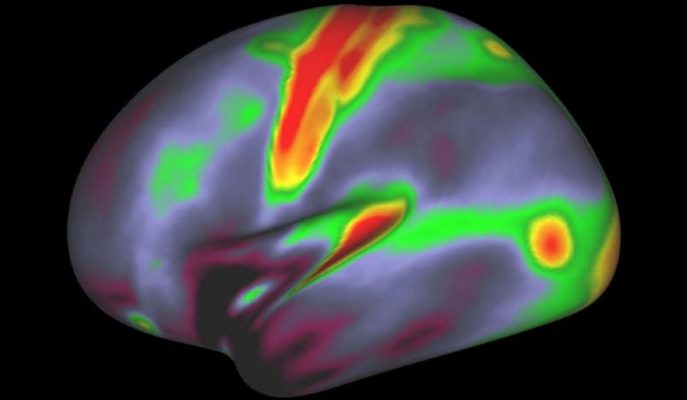
Un futuro más nítido
El equipo ahora se está preparando para una tercera ronda de expansión, que hipotéticamente permitiría una resolución de 5 nanómetros. El bloqueo está encontrando sondas fluorescentes lo suficientemente pequeñas que pueden apretarse juntas para trabarse en dos proteínas cercanas antes de expandirse. Alternativamente, los científicos también podrían desarrollar nuevas sondas que etiqueten sus proteínas después de la expansión.
Mientras que conseguir imágenes más nítidas es grande, la meta final es poder seguir el cableado de circuitos completos del cerebro, dice Boyden.
Ya tiene una idea: multiplexación temporal. En la actualidad, solo unas cuantas sondas coloreadas se pueden utilizar para imágenes de proteínas en una muestra-una vez y hecho.
El multiplexamiento temporal convierte esencialmente el tejido en multiuso. Los investigadores pueden etiquetar un grupo de proteínas como de costumbre, la imagen del tejido, luego quitar las sondas y volver a conectar los nuevos.
Esto permite que un número exponencial de proteínas sea probado con cada ronda, dicen los investigadores.
«Al combinar la expansión iterativa con la multiplexación temporal, en principio podríamos tener imágenes de resolución en nanoescala a escala de infinito color sobre grandes volúmenes tridimensionales«, dice Boyden. «Las cosas se están poniendo realmente emocionantes ahora que estas diferentes tecnologías pronto podrían conectarse entre sí«.